O que é o sistema
O Sistema de Identificação Única de Dispositivos Médicos (UDI)/Unique Device Identification (UDI) é um padrão internacional que pretende se consolidar como um sistema global e harmozinado de identificação de produtos médicos, conforme a sua distribuição e uso nos pacientes, estabelecendo uma garantia de rastreabilidade e um sistema de vigilância globalizado. É um modelo baseado nas diretrizes do IMDRF (International Medical Device Regulators Forum) e já aplicado dentro de agências regulatórias em países como os EUA, o Japão e a Coreia do Sul.
O Sistema de identificação UDI envolve também a criação de uma base de dados pública pela agência regulatória.
O que é UDI
Conforme o Guia do IMDRF sobre o assunto, o UDI é uma sequência numérica ou alfanumérica, criada por meio de uma identificação de dispositivos globalmente aceita e um padrão de codificação, que é formada por duas partes: DI e PI, e é afixada na rotulagem e/ou no próprio produto.
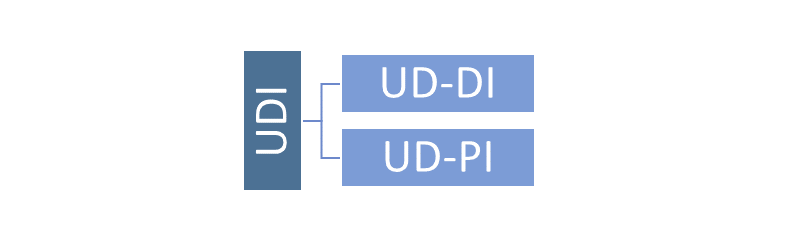
O UDI-DI (Device Identifier) é um código de identificação específico de um modelo de dispositivo (portanto, um código fixo entre produtos de um mesmo modelo) e reúne informações como, por exemplo, o número GTIN.
O UDI-PI (Production Identifier) é um código variável e referencia os dados de fabricação, como, por exemplo, data de fabricação e validade, lote, número de série, etc.
Esses caracteres combinados permitem a identificação inequívoca de um determinado dispositivo médico no mercado, assegurando assim a segurança do paciente em diversos níveis e facilitando a logística da cadeia de distribuição.
O Sistema UDI e a ANVISA
A Consulta Pública nº 1.051/2021, que abrange uma proposta de Resolução de Diretoria Colegiada RDC que dispõe sobre a identificação positiva de dispositivos médicos regularizados na Anvisa, por meio do sistema de Identificação Única de Dispositivos Médicos (UDI), ficou aberta ao público para contribuições até o começo de setembro (06/09/2021).
A última previsão da Agência é de que em Dezembro/2021 ocorreria a apreciação da Diretoria Colegiada da Anvisa, e consequentemente a publicação da RDC.
Questões relevantes sobre o tema
Quais tipos de produtos médicos precisarão de UDI conforme a consulta pública?
A proposta de resolução da Anvisa é direcionada aos produtos médicos e os produtos para diagnóstico in vitro, regulados pela RDC nº 185/2001, RDC nº 36/2015, e RDC nº 40/2015, excetuando-se apenas os dispositivos médicos feitos sob medida e dispositivos médicos em investigação clínica.
Quais são os prazos de implementação conforme a consulta pública?
O Art. 15. da Consulta Pública nº 1.051/2021 coloca que, os prazos para atribuir a UDI e aplicar os suportes da UDI, após a data de início da vigência da Resolução, serão de:
- 2 anos para os dispositivos médicos de classe de risco IV;
- 3 anos para os dispositivos médicos de classe de risco III;
- 4 anos para os dispositivos médicos de classe de risco II;
- 6 anos para os dispositivos médicos de classe de risco I.
Ademais, a Consulta traz ainda diversos detalhes quanto a esses prazos, vale a pena a leitura se você é fabricante, importador e/ou distribuidor de produtos médicos.
E a disponibilização de informações na Base de Dados UDI da Anvisa?
A submissão de dados segue o mesmo escalonamento da atribuição de UDI e suportes, porém iniciando a contagem a partir do momento em que a Anvisa publicar em instrução normativa que a base de dados UDI da Agência está apta a receber as informações.
Quais são as entidades emissoras de UDI?
A Consulta Pública nº 1.051/2021 prevê inicialmente que as entidades emissoras serão:
- GS1
- HIBCC (Health Industry Business Communications Council);
- ICCBBA (International Council for Commonality in Blood Banking Automation).
Colaboração: Equipe de Estratégia em Produto Regulado
Segmento de interesse: Produtos para Saúde
Referências Bibliográficas: www.gov.br/anvisa/pt-br
Sistema de Identificação Única de Dispositivos Médicos (UDI) e a CP nº 1.051/2021





